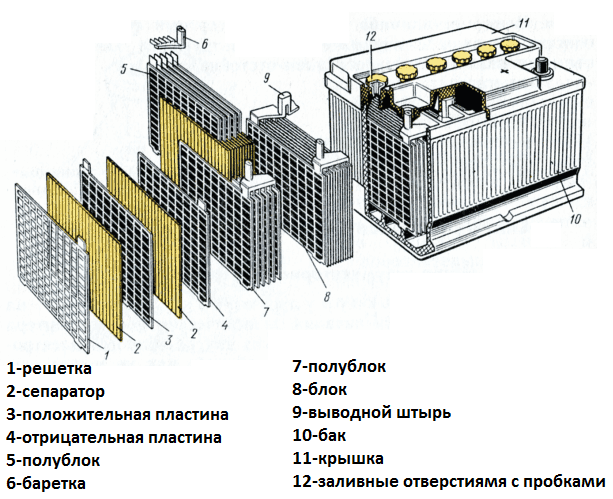
Аккумулятор – это устройство, которое способно преобразовывать химическую энергию в электрическую. Он служит для временного хранения источника электричества, который в дальнейшем можно использовать в различных портативных устройствах и электротранспорте. Принцип работы аккумулятора основан на реакциях окисления и восстановления внутри его структуры.
Основными элементами аккумулятора являются два электрода – катод и анод, которые разделены электролитом. Катод – это электрод, на котором происходит окисление, а анод – электрод, на котором происходит восстановление. Именно благодаря этим реакциям происходит накопление и передача энергии в аккумуляторе.
Процесс работы аккумулятора начинается с подключения его к внешнему источнику электричества, например, зарядному устройству. Во время зарядки на аноде происходит окисление активного материала, который обогащается положительно заряженными частицами. Таким образом, происходит образование свинцовой оксидной пасты на аноде.
После полной зарядки аккумулятора, он готов к использованию. В процессе выработки аккумулятора на катоде происходит обратная реакция, в результате которой свинцовая оксидная паста восстанавливается, а свинец и серная кислота возвращаются в исходное состояние. Это происходит благодаря движению электрических зарядов между катодом и анодом через электролит.
Устройство и принцип работы аккумулятора: основные принципы и структура
Структура аккумулятора состоит из двух электродов — положительного и отрицательного, разделенных электролитом. Положительный электрод часто называют катодом, а отрицательный — анодом.
Ключевым элементом аккумулятора являются электрохимические реакции, происходящие на электродах. При зарядке аккумулятора на аноде происходит окисление активного материала, который обычно представлен свинцом. В результате электрохимической реакции образуется положительно заряженный ион свинца, который перемещается через электролит к катоду, преобразуя электрическую энергию.
На катоде происходит редукция активного материала, который может состоять из пероксида свинца или кислорода. В результате данной реакции образуются свинец или вода, а также свободные электроны, которые перемещаются по внешней электрической цепи, что создает электрический ток.
В процессе разряда аккумулятора электрохимические реакции на электродах протекают в обратном направлении. Происходит окисление на катоде и редукция на аноде, что приводит к высвобождению химической энергии и созданию электрического тока.
Основными принципами работы аккумулятора являются возможность повторной зарядки и разрядки, а также возможность многократного использования аккумулятора без значительной потери его свойств. Это делает аккумуляторы одним из наиболее удобных и эффективных источников электроэнергии в различных электроприборах.
Принцип работы аккумулятора
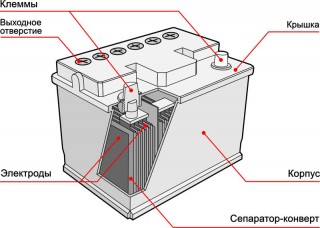
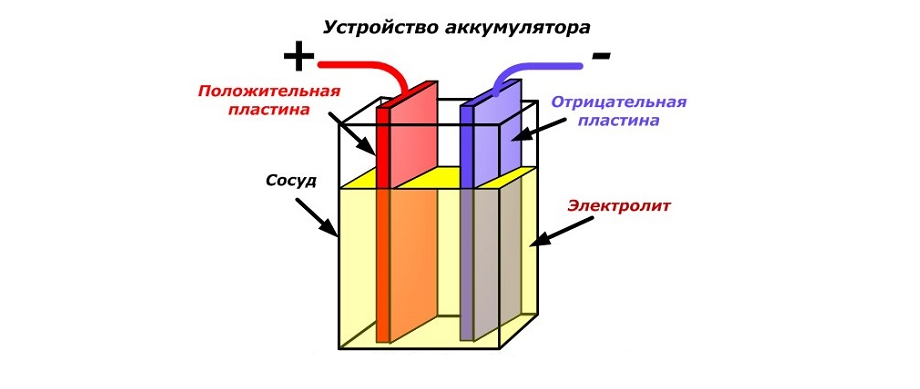
Структура аккумулятора включает в себя положительный и отрицательный электроды, разделенные электролитом, который является проводником для ионов. Когда аккумулятор заряжается, происходит окисление вещества на положительном электроде и восстановление на отрицательном электроде. При этом ионы перемещаются через электролит. Во время разряда аккумулятора, реакции происходят в обратном направлении – окисление вещества на отрицательном электроде и восстановление на положительном.
Преимущество аккумуляторов заключается в их перезаряжаемости. При использовании внешнего источника электрической энергии, например, солнечных панелей или генератора, аккумулятор может быть заряжен снова. Это делает их удобными и экономически эффективными для использования в различных устройствах, таких как мобильные телефоны, ноутбуки, электромобили и другие.
Таблица ниже показывает основные характеристики различных типов аккумуляторов:
| Тип аккумулятора | Преимущества | Недостатки |
|---|---|---|
| Свинцово-кислотный (например, автомобильный аккумулятор) | Низкая стоимость, высокая емкость | Тяжелый, требует обслуживания и правильной зарядки |
| Литий-ионный (например, аккумуляторы для ноутбуков и смартфонов) | Высокая энергетическая плотность, нет эффекта памяти, малый саморазряд | Высокая стоимость, необходимость в специальной электронике для управления зарядом и разрядом |
| Никель-кадмиевый | Высокая емкость, стабильная работа на большом диапазоне температур | Высокая стоимость, содержит кадмий, которые является вредным веществом |
В зависимости от конкретного применения, выбираются подходящие типы аккумуляторов, учитывая их характеристики, стоимость и другие факторы. Важно также следить за правильной эксплуатацией и обслуживанием аккумуляторов, чтобы обеспечить их долговечность и безопасность использования.
Основные принципы
Принцип работы аккумулятора основан на электрохимических реакциях, происходящих внутри его ячеек. Обычно аккумуляторы состоят из положительного и отрицательного электродов, разделенных электролитом.
При зарядке аккумулятора происходит химическая реакция, в результате которой электроны отталкиваются от положительного электрода и перемещаются на отрицательный электрод через внешнюю цепь. В процессе разрядки аккумулятора происходит обратная реакция, в результате которой электроны движутся отрицательного электрода к положительному через внешнюю цепь, создавая электрический ток.
У аккумулятора есть определенная емкость и напряжение, которые определяют его способность запоминать и выдавать энергию. Для эффективной работы аккумулятор должен быть правильно заряжен и разряжен, чтобы поддерживать его производительность и продлевать срок службы.
Химическая реакция
Аккумулятор представляет собой устройство, внутри которого происходят химические реакции. Эти реакции происходят между различными химическими веществами, называемыми электролитами. В аккумуляторе применяются различные типы электролитов, такие как свинцово-кислотный электролит (PbSO4), никель-кадмиевый электролит (NiCd), литий-ионный электролит (Li-ion) и другие.
Химическая реакция, происходящая в аккумуляторе, осуществляется за счет перемещения электронов между электродами. Аккумулятор состоит из позитивного и негативного электродов, которые погружены в электролит. При зарядке аккумулятора химическая энергия преобразуется в электрическую энергию, а при разрядке — наоборот.
В процессе химической реакции при зарядке аккумулятора происходит окисление и восстановление веществ на электродах. На позитивном электроде происходит реакция окисления, а на негативном электроде — реакция восстановления. Это позволяет накапливать энергию в аккумуляторе и использовать ее по мере необходимости.
Одной из ключевых составляющих химической реакции, происходящей в аккумуляторе, является электролит. Он играет роль проводника для электрического тока и обеспечивает перемещение ионов между электродами. В зависимости от типа аккумулятора, электролит может быть жидким или гелевым.
- Жидкий электролит представляет собой раствор химических веществ в воде или другом растворителе. Он обеспечивает химические реакции на электродах и ионную проводимость в аккумуляторе.
- Гелевый электролит содержит гельобразную субстанцию, которая удерживает электролит в виде желе. Он используется, например, в гелевых свинцово-кислотных аккумуляторах.
Химическая реакция, происходящая в аккумуляторе, довольно сложна и может быть представлена рядом уравнений, объединенных в рамках электрохимической теории. В процессе разрядки аккумулятора происходит обратная реакция, при которой электрическая энергия преобразуется в химическую энергию.
Таким образом, химическая реакция является основной причиной работы аккумулятора. Она позволяет накапливать и хранить энергию, которую затем можно использовать для питания различных устройств.
Процесс зарядки и разрядки
В процессе зарядки аккумулятора, электрическая энергия из внешнего источника подается на положительный и отрицательный электроды аккумулятора. В результате этого происходит химическая реакция, которая превращает электрохимические реагенты в активные соединения, способные накапливать энергию. При этом, электрические заряды перемещаются от положительного электрода к отрицательному через проводящую среду.
В процессе разрядки аккумулятора, химические соединения в аккумуляторе превращаются обратно в электрохимические реагенты, освобождая при этом накопленную энергию. При разрядке, происходит обратное направление движения электрических зарядов, от отрицательного электрода к положительному, при этом предоставляя энергию для использования.
Процесс зарядки и разрядки аккумулятора осуществляется множеством химических реакций, происходящих внутри аккумулятора, что позволяет использовать аккумулятор для накопления и выделения энергии во многих устройствах.
Структура аккумулятора
1. Электроды: аккумулятор содержит два электрода — положительный (катод) и отрицательный (анод). Они выполнены из разных химических веществ и играют важную роль в процессе химической реакции, происходящей во время зарядки и разрядки аккумулятора.
2. Электролит: это вещество, наполненное между электродами, которое позволяет ионам двигаться между ними во время химической реакции. Обычно для аккумуляторов используется жидкий электролит, состоящий из различных солей или кислоты.
3. Сепаратор: это слой материала, который разделяет положительный и отрицательный электроды. Он позволяет ионам проходить, но предотвращает контакт между электродами, чтобы избежать короткого замыкания.
4. Корпус: аккумулятор обычно имеет внешний корпус, который защищает его от повреждений и предотвращает утечку электролита. Корпус часто выполнен из металла или пластика.
5. Терминалы: это металлические контакты на концах аккумулятора, которые используются для подключения к электрической цепи. Через терминалы происходит передача электроэнергии между аккумулятором и другими электрическими устройствами.
6. Защитные системы: некоторые аккумуляторы могут быть оборудованы дополнительными системами безопасности, такими как предохранители или защитные цепи, чтобы предотвратить перегрузку или короткое замыкание.
Все эти компоненты работают вместе, чтобы обеспечить функционирование аккумулятора и его способность хранить и выдавать электрическую энергию при необходимости.
| Компонент | Функция |
|---|---|
| Электроды | Позволяют химическим реакциям происходить в аккумуляторе, создавая и сохраняя электрическую энергию |
| Электролит | Позволяет ионам двигаться между электродами и запускает химические реакции |
| Сепаратор | Предотвращает короткое замыкание, разделяя положительный и отрицательный электроды |
| Корпус | Защищает аккумулятор и предотвращает утечку электролита |
| Терминалы | Соединяют аккумулятор с другими устройствами и передают электроэнергию |
| Защитные системы | Предотвращают перегрузку или короткое замыкание в аккумуляторе |
Типы аккумуляторов
Существует несколько типов аккумуляторов, каждый из которых обладает своими особенностями и применением. Вот некоторые из них:
| Тип аккумулятора | Описание | Применение |
|---|---|---|
| Свинцово-кислотный (СКА) | Аккумуляторы данного типа используются повсеместно благодаря своей надежности и низкой стоимости. Они состоят из свинцовых пластин, разделенных слоями пористых материалов, пропитанных серной кислотой. | Часто применяются в автомобилях и других транспортных средствах, стационарных и резервных источниках энергии. |
| Никель-кадмиевый (NiCd) | Аккумуляторы этого типа обладают высокой плотностью энергии и способностью к быстрой зарядке. Однако они содержат вредные вещества, такие как кадмий, и имеют эффект «памяти». | Часто используются в портативных устройствах, таких как ноутбуки, электроинструменты и радиоприемники. |
| Литий-ионный (Li-ion) | Литий-ионные аккумуляторы обладают высокой энергетической плотностью, низким саморазрядом и отсутствием эффекта «памяти». Однако они более чувствительны к повышенным температурам и могут быть опасными при неправильном использовании. | Широко используются в смартфонах, ноутбуках, планшетах и других портативных электронных устройствах. |
| Литий-полимерный (Li-Po) | Литий-полимерные аккумуляторы имеют гибкую и тонкую структуру, что позволяет создавать более компактные и тонкие устройства. Они также обладают высокой энергетической плотностью и не содержат жидких электролитов. | Широко применяются в смартфонах, планшетах, ноутбуках и других устройствах, где требуется малый объем и легкий вес аккумулятора. |
Каждый из этих типов аккумуляторов имеет свои преимущества и недостатки, и выбор правильного типа зависит от конкретных требований и условий эксплуатации.
Литий-ионные аккумуляторы
Основным элементом Li-ion аккумулятора является литий-ионная батарея, состоящая из положительного катода, отрицательного анода и электролита между ними. В отличие от других типов аккумуляторов, Li-ion аккумуляторы не содержат в себе свинец, кадмий или ртуть, что делает их более экологически безопасными и удобными в использовании.
Основной принцип работы Li-ion аккумуляторов заключается в переносе литий-ионов между катодом и анодом во время процесса зарядки и разрядки. При зарядке аккумулятора литий-ионы перемещаются с катода на анод, а при разрядке — с анода на катод.
Одним из главных преимуществ Li-ion аккумуляторов является их высокая энергоемкость. Они способны хранить большое количество энергии на небольшом пространстве. Кроме того, Li-ion аккумуляторы отличаются высокой скоростью зарядки и низкой саморазрядкой, что делает их очень удобными в использовании.
Также стоит отметить, что Li-ion аккумуляторы не требуют периодического формирования и могут быть заряжены в любое время, не образуя «эффект памяти». Однако, они требуют мониторинга и контроля температуры, чтобы избежать перегрева и повреждений.
В целом, Li-ion аккумуляторы являются важной частью нашей современной технологии и находят применение в широком спектре устройств, начиная от мобильных телефонов и ноутбуков, до электромобилей и солнечных батарей. Они предлагают множество преимуществ и продолжают развиваться, чтобы удовлетворить растущие потребности нашего мира в энергии.
| Преимущества | Недостатки |
|---|---|
| Высокая энергоемкость | Возможность перегрева |
| Высокая скорость зарядки | Ограниченное количество циклов зарядки/разрядки |
| Низкая саморазрядка | Высокая стоимость |
Преимущества и недостатки
Преимущества аккумуляторов:
1. Возобновляемая энергия: аккумуляторы позволяют эффективно использовать возобновляемые источники энергии, такие как солнечные и ветряные установки.
2. Переносимость: аккумуляторы являются портативными, что делает их удобными для использования в различных ситуациях, включая путешествия и кемпинг.
3. Длительное время работы: некоторые типы аккумуляторов способны обеспечивать длительное время работы, что особенно важно для устройств, которые требуют постоянного питания, например, мобильных телефонов и ноутбуков.
4. Не требуют постоянной замены: аккумуляторы могут быть повторно заряжены множество раз, что позволяет избежать постоянной покупки и замены батареек.
Недостатки аккумуляторов:
1. Ограниченный срок службы: аккумуляторы со временем теряют свою емкость, что приводит к уменьшению времени работы и необходимости замены.
2. Затраты на замену: в некоторых случаях, когда аккумуляторы выходят из строя, их замена может быть дорогостоящей.
3. Необходимость периодической зарядки: аккумуляторы требуют регулярной зарядки, что может быть неудобно при использовании в отдаленных местах без доступа к электричеству.
4. Экологические проблемы: некоторые типы аккумуляторов содержат вредные вещества, которые могут нанести ущерб окружающей среде, если они не утилизированы правильно.
Никель-кадмиевые аккумуляторы
Структура никель-кадмиевого аккумулятора состоит из пластинок кадмия и никеля, разделенных сепараторами и погруженных в электролит. Пластины кадмия и никеля служат в качестве анода и катода соответственно. Электролит обычно представляет собой раствор щелочи.
Принцип работы НКА заключается в процессе химических реакций на пластинах кадмия и никеля. Во время разряда аккумулятора, катод (никель) осуществляет окислительные реакции, анод (кадмий) — восстановительные. Происходит переход электронов через внешнюю цепь, что создает электрическую энергию.
Одной из особенностей никель-кадмиевого аккумулятора является его высокая энергетическая плотность, что позволяет обеспечивать высокий уровень энергии на единицу массы аккумулятора. Это делает НКА привлекательным для использования в портативных устройствах, где важно иметь компактный и легкий источник питания.
Однако, никель-кадмиевые аккумуляторы имеют ряд недостатков. Они подвержены «эффекту памяти», что означает, что аккумулятор может «запомнить» предыдущую низкую зарядку и не сможет полностью зарядиться в дальнейшем. Также, НКА обладают небольшим саморазрядом, что приводит к потере энергии со временем даже при отсутствии использования.
В целом, никель-кадмиевые аккумуляторы предоставляют надежный и эффективный источник питания для множества устройств. Они обладают высокой энергетической плотностью и широким диапазоном рабочих условий. Несмотря на некоторые недостатки, НКА остаются популярными и широко применяемыми в современных технологиях.
Преимущества и недостатки
- Повторное использование: аккумуляторы могут быть перезаряжены и использованы множество раз, что позволяет экономить ресурсы и снижать количество отходов.
- Портативность: аккумуляторы обычно компактны и легки, что делает их удобными в использовании в различных устройствах, от мобильных телефонов до электронных автомобилей.
- Эффективность: аккумуляторы обладают высокой энергетической плотностью, что позволяет им хранить большое количество энергии на небольшом пространстве.
- Быстрая зарядка: современные технологии позволяют быстро заряжать аккумуляторы, что делает их очень удобными в использовании в повседневной жизни.
- Уменьшение выбросов: использование аккумуляторов вместо одноразовых батареек позволяет снизить количество отходов и негативное воздействие на окружающую среду.
Хотя аккумуляторы обладают множеством преимуществ, они также имеют некоторые недостатки:
- Ограниченный срок службы: аккумуляторы не могут бесконечно долго использоваться и со временем их производительность снижается.
- Надежность: некачественные или поврежденные аккумуляторы могут стать причиной возникновения проблем и даже опасных ситуаций, таких как перегрев или взрыв.
- Зависимость от зарядки: для использования аккумуляторов они должны быть периодически заряжены, что может быть неудобно и требовать наличия доступа к электрической сети.
- Высокая стоимость: некоторые типы аккумуляторов могут быть довольно дорогими по сравнению с одноразовыми батарейками, что может быть фактором при выборе.
В целом, аккумуляторы являются важным и удобным источником энергии с множеством преимуществ, но также имеют свои недостатки, которые необходимо учитывать при их использовании.
Свинцово-кислотные аккумуляторы
Основная структура свинцово-кислотных аккумуляторов включает в себя положительные и отрицательные электроды, а также электролит, который обеспечивает перемещение ионов внутри аккумулятора.
Положительный электрод состоит из свинца и свинцового диоксида, а отрицательный электрод — из свинца и свинцового гидроксида. Электролитом, как правило, является раствор серной кислоты.
Принцип работы свинцово-кислотного аккумулятора основан на химической реакции, происходящей при зарядке и разрядке аккумулятора. Во время зарядки происходит превращение свинца и свинцового гидроксида в свинец и свинцовый диоксид, а при разрядке — обратная реакция.
Преимущества свинцово-кислотных аккумуляторов — низкая стоимость, большая емкость и способность выделять высокий ток. Однако они обладают недостатками, такими как большой вес, небольшая энергетическая плотность и ограниченное количество циклов зарядки и разрядки.
Свинцово-кислотные аккумуляторы являются широко распространенными в настоящее время, но с развитием технологий появляются новые типы аккумуляторов, которые обладают более высокой энергетической плотностью и длительным сроком службы. Однако свинцово-кислотные аккумуляторы все еще остаются востребованными благодаря своей надежности и доступности.
Преимущества и недостатки аккумуляторов
- Преимущества:
- Экологическая чистота – аккумуляторы не содержат вредных веществ, таких как свинец или кадмий, что делает их безопасными для окружающей среды.
- Невысокая стоимость эксплуатации – аккумуляторы можно перезаряжать, что позволяет использовать их в течение длительного времени без необходимости покупки новых батарей или элементов питания.
- Гибкость в применении – аккумуляторы могут использоваться в различных устройствах, начиная от малогабаритных электронных гаджетов до транспортных средств и систем энергоснабжения.
- Высокая энергоемкость – современные аккумуляторы способны хранить большое количество энергии и обеспечивать длительное время автономной работы устройств.
- Возможность быстрой зарядки – некоторые типы аккумуляторов, например, литий-ионные аккумуляторы, позволяют быстро заряжать устройства и минимизировать время простоя.
- Недостатки:
- Ограниченный ресурс – аккумуляторы имеют ограниченное количество циклов зарядки/разрядки, после чего их энергетическая емкость снижается.
- Саморазрядка – даже при отсутствии использования аккумуляторы со временем теряют свою зарядку, что может быть проблемой при хранении.
- Опасность перезарядки – неправильная эксплуатация аккумуляторов, такая как перезарядка или короткое замыкание, может вызвать их перегрев, взрыв или пожар.
- Чувствительность к температуре – аккумуляторы могут быстрее разряжаться при низких температурах, а также их работоспособность может снижаться при высоких температурах.
- Ограниченный выбор – не все устройства могут быть совместимы с аккумуляторами, и некоторые требуют специальные типы или размеры аккумуляторов.
Применение аккумуляторов
Аккумуляторы широко применяются в различных областях, где требуется независимое источник питания. Вот несколько основных областей применения аккумуляторов:
Телекоммуникации: Аккумуляторы используются в системах связи и сотовых телефонах, обеспечивая энергией их работу и позволяя осуществлять безперебойную связь.
Автомобильная промышленность: Аккумуляторы играют важную роль в автомобилях для питания системы зажигания, освещения и других электрических устройств.
Авиация и космос: В самолетах и космических аппаратах аккумуляторы необходимы для обеспечения работы электрических систем и приборов.
Энергетическая отрасль: Аккумуляторы используются в солнечных и ветряных батареях для сохранения и распределения электрической энергии.
Бытовая техника: Многие бытовые устройства, такие как ноутбуки, мобильные телефоны, планшеты и электрические инструменты, работают от аккумуляторов, обеспечивая их мобильность и независимость от сети.
Это лишь некоторые примеры применения аккумуляторов. Они также используются в робототехнике, медицинском оборудовании, системах резервного питания и других отраслях, где электрическая энергия является неотъемлемой частью работы и функционирования устройств.